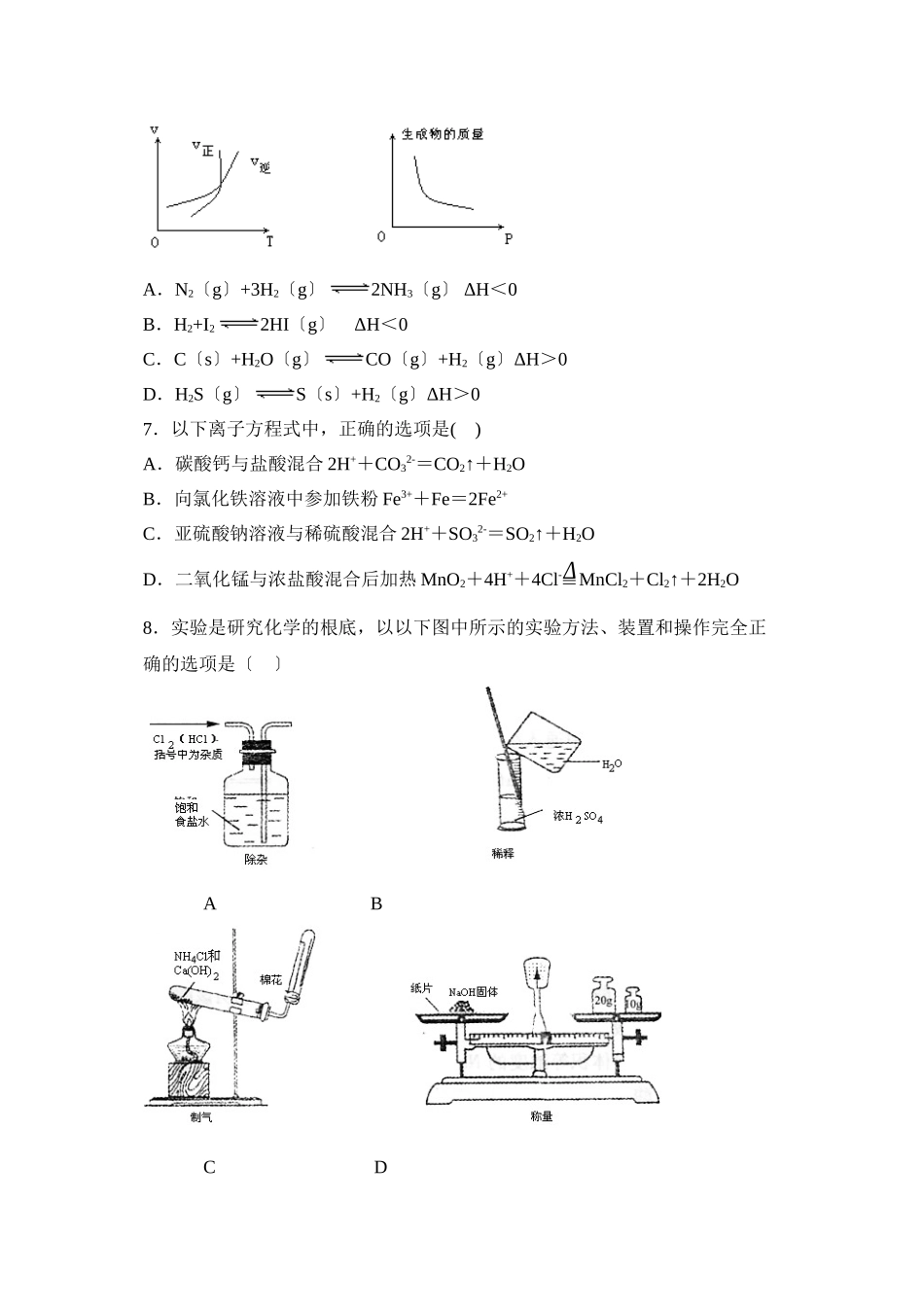
高三期中考试化学试题寄语:细节决定成败,慎思表达素质,标准凸现成绩可能用到的原子量:H1O16Na23Mg24Al27Cl35.5Fe56Cu64Zn65S32Ⅰ卷〔共50分〕一、选择题:(此题有10个小题,每题只有1个选项正确,每题2分,共20分)1.起固定氮作用的化学反响是()A.NH3与NO在一定条件下反响生成N2B.硝酸工厂用NH3氧化制NOC.雷雨时空气中的N2转化为NOD.由NH3制碳酸氢铵和硫酸铵2.把一小块钠投入盛有煤油和水的烧杯中,可以观察到的现象是()A.钠浮在烧杯中的液面上B.钠沉在烧杯的底部C.钠会在水和煤油的交界面上下浮动,直到反响结束D.煤油会燃烧起来,产生很浓的黑烟3.以下关于浓HNO3与浓H2SO4的表达正确的选项是〔〕A.常温下都可用锌制容器贮存B.常温下都能与铜较快反响C.露置于空气中,溶液质量均减轻D.露置于空气中,溶液浓度均降低4.以下变化不可能通过一步实验直接完成的是〔〕A.Al(OH)3→Al2O3B.Al2O3→Al(OH)3C.Al→[Al(OH)4]-D.Al3+→Al(OH)35“.某学生设计了一个黑笔写红字〞的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,以下表达正确的选项是()A.铅笔端作阳极,发生复原反响B.铂片端作阴极,发生氧化反响C.铅笔端有少量的氯气产生D.a点是负极,b点是正极6.如以下图为在一定条件下进行的可逆反响,当改变其中一个条件时的图象变化曲线。那么图象表示的可逆反响为〔〕铂片滤纸铅笔祝你成功ab直流电源A.N2〔g〕+3H2〔g〕2NH3〔g〕ΔH<0B.H2+I22HI〔g〕ΔH<0C.C〔s〕+H2O〔g〕CO〔g〕+H2〔g〕ΔH>0D.H2S〔g〕S〔s〕+H2〔g〕ΔH>07.以下离子方程式中,正确的选项是()A.碳酸钙与盐酸混合2H++CO32-=CO2↑+H2OB.向氯化铁溶液中参加铁粉Fe3++Fe=2Fe2+C.亚硫酸钠溶液与稀硫酸混合2H++SO32-=SO2↑+H2OD.二氧化锰与浓盐酸混合后加热MnO2+4H++4Cl-ΔMnCl2+Cl2↑+2H2O8.实验是研究化学的根底,以以下图中所示的实验方法、装置和操作完全正确的选项是〔〕ABCD209.为了除去氯气中混有的少量水蒸气,可使含杂质的氯气通过某特定的枯燥管,此枯燥管中装有以下药品中的()A.五氧化二磷B.浓硫酸C.饱和食盐水D.碱石灰10.阿伏加德罗常数约为6.02×1023mol-1,以下说法中一定正确的选项是〔〕A.1molFeCl3完全转化为Fe(OH)3胶体后生成6.02×1023个胶粒B.标准状况下,2.24L乙醇完全燃烧所得CO2分子数为0.2×6.02×1023C.1L0.1mol·L...