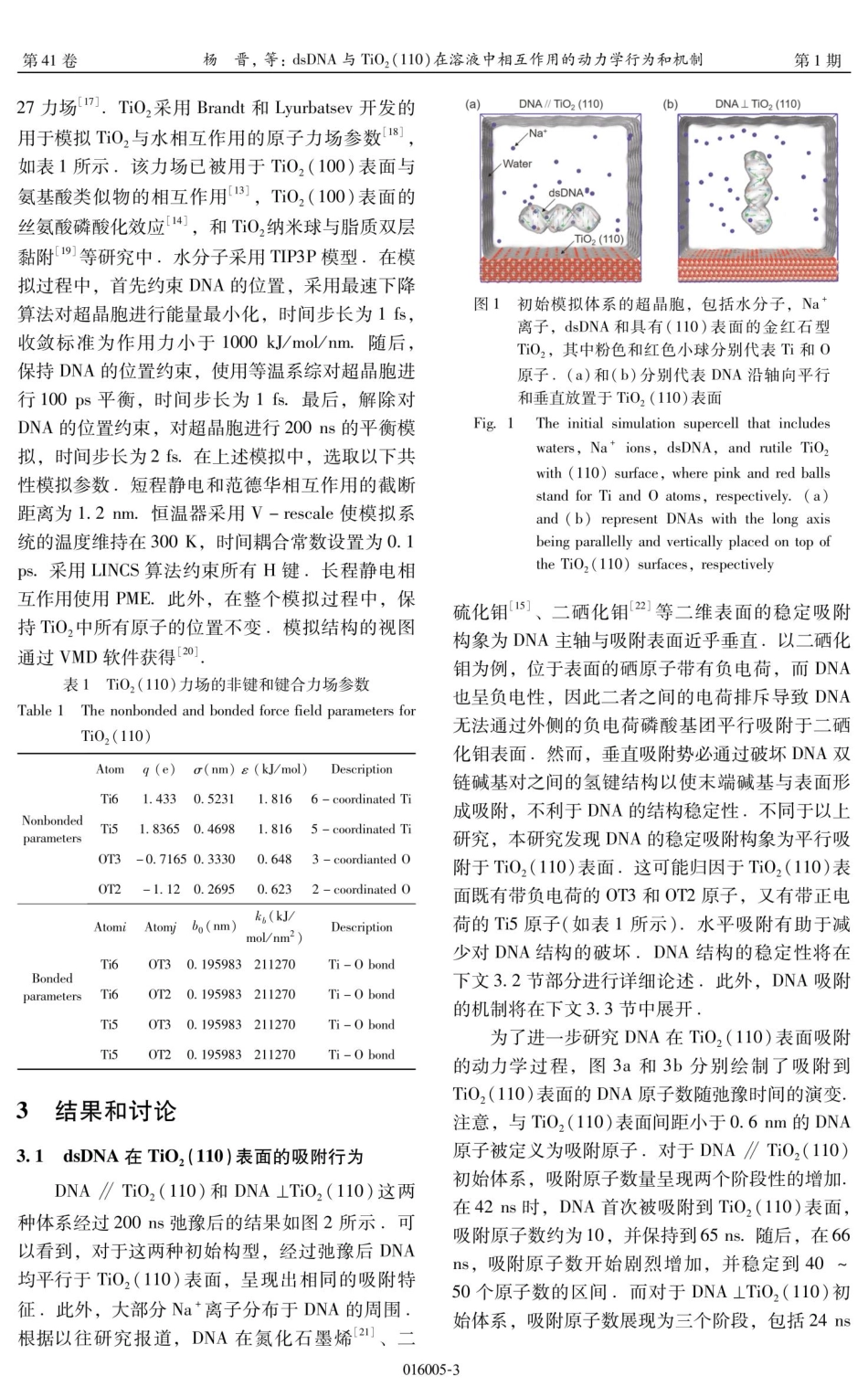
第41卷第1期2024年2月J.At.Mol.Phys.,2024,41:016005(7pp)原子与分子物理学报JOURNALOFATOMICANDMOLECULARPHYSICSdsDNA与TiO,(110)在溶液中相互作用的动力学行为和机制杨晋2.3,胡书环3,刘雯,孟范超Vol.41No.1Feb.2024(1.中国科学院大学生命科学学院,北京100049;2.深圳华大生命科学研究院,深圳518083;3.广东省高通量测序工程技术研究中心,深圳518083;4.康年医疗科技有限公司,山东烟台264030;5.烟台大学精准材料高等研究院,烟台264005)摘要:金红石型TiO,(110)在DNA传感领域具有广阔的应用前景,然而其与DNA在溶液中相互作用的动力学行为和机制尚不清楚,利用分子动力学模拟,深入研究了双链DNA(dsDNA)在初始时沿轴向平行或垂直于金红石型TiO2(110)表面时二者在溶液中的相互作用,通过分析dsDNA在吸附后的稳定构型、吸附动力学过程和结构稳定性发现,与一些典型二维纳米材料不同,dsDNA倾向于水平吸附到TiO2(110)表面.水平吸附不仅使得dsDNA的四种碱基均吸附到TiO2(110)表面,增加了吸附稳定性,而且不破坏ds-DNA的结构稳定性.进而,通过分析dsDNA与TiO,(110)表面的相互作用能和水分子密度/数量发现,dsD-NA的平行吸附可能源于二者之间的短程范德华和长程静电相互作用:此外,纳米级脱湿也增强了dsDNA的吸附。对dsDNA与TiO,(110)在溶液中的相互作用研究有助于实现TiO,(110)在DNA传感中的应用关键词:过渡族金属氧化物;TiO2;dsDNA;相互作用机制;分子动力学模拟中图分类号:TQ134ThedynamicbehaviorandmechanismunderlyingtheinteractionbetweendsDNAandTiO,(110)insolution文献标识码:AD0I:10.19855/j.1000-0364.2024.016005YANGJin'2.3,HUShu-Huan?3,LIUWent,MENGFan-Chao"(1.CollegeofLifeSciences,UniversityofChineseAcademyofSciences,Beijing100049,China;2.BGI-Shenzhen,Shenzhen518083,China;3.GuangdongHigh-throughputSequencingResearchCenter,Shenzhen518083,China;4.KangnianMedicalTechnologiesCo.,Ltd.,Yantai264030,China;5.InstituteforAdvancedStudiesinPrecisionMaterials,YantaiUniversity,Yantai264005,China)Abstract:RutileTiO,(110)isapromisingmaterialforapplicationsinDNAsensing.However,thedynamicbe-haviorandmechanismofitsinteractionwithDNAinsolutionremainunclear.Employingmoleculardynamicssimulations,thepresentpaperexaminestheinteractionbetweendouble-strandedDNA(dsDNA)andrut...