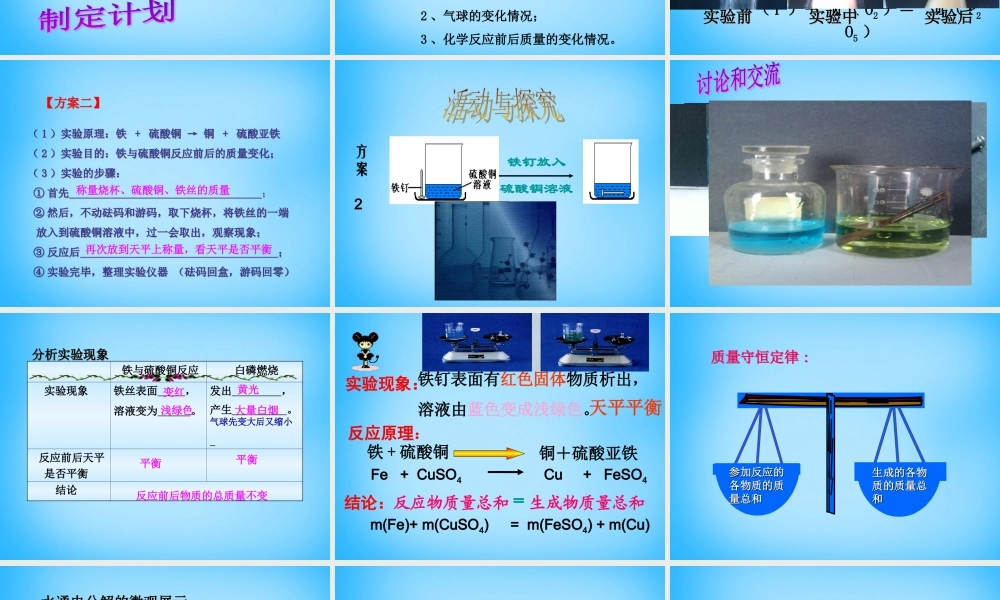
课题1质量守恒定律课题1质量守恒定律第五单元化学方程式第五单元化学方程式生日宴会中我们发现生日蜡烛会越烧越短。金属生锈后质量变大了。1、结合生活中遇到的现象,提出问题:化学反应前后物质的质量有没有变化呢?2、你的猜想是(变大、变小、或不变);一、质量守恒定律一、质量守恒定律物质在发生化学变化时,反应物的质量总和与生成物的质量总和之间存在什么关系呢?生成物的质量总和反应物的质生成物的质量总和反应物的质量总和量总和等于等于大于大于小于小于玻璃管注意观察:1、锥形瓶内白磷燃烧的现象;2、气球的变化情况;3、化学反应前后质量的变化情况。白磷燃烧前后质量总和的测定方案方案11细沙剧烈燃烧,产生大量白烟,放出大量热气球先鼓起后瘪掉,文字表达式:磷+氧气点燃五氧化二磷结论:反应物质量总和生成物质量总和现象:天平仍保持平衡天平仍保持平衡。。m(P)+m(O2)=m(P2O5)=实验前实验前实验中实验中实验后实验后(1)实验原理:铁+硫酸铜→铜+硫酸亚铁(2)实验目的:铁与硫酸铜反应前后的质量变化;(3)实验的步骤:①首先;②然后,不动砝码和游码,取下烧杯,将铁丝的一端放入到硫酸铜溶液中,过一会取出,观察现象;③反应后;④实验完毕,整理实验仪器(砝码回盒,游码回零)(1)实验原理:铁+硫酸铜→铜+硫酸亚铁(2)实验目的:铁与硫酸铜反应前后的质量变化;(3)实验的步骤:①首先;②然后,不动砝码和游码,取下烧杯,将铁丝的一端放入到硫酸铜溶液中,过一会取出,观察现象;③反应后;④实验完毕,整理实验仪器(砝码回盒,游码回零)称量烧杯、硫酸铜、铁丝的质量再次放到天平上称量,看天平是否平衡【方案二】【方案二】方案2铁钉放入硫酸铜溶液铁与硫酸铜反应白磷燃烧实验现象铁丝表面,溶液变为。发出,产生。气球先变大后又缩小反应前后天平是否平衡结论平衡反应前后物质的总质量不变平衡黄光浅绿色大量白烟变红分析实验现象分析实验现象实验现象:反应原理:铁+硫酸铜铜+硫酸亚铁结论:反应物质量总和=生成物质量总和铁钉表面有红色固体物质析出,溶液由蓝色变成浅绿色。Fe+CuSO4Cu+FeSO4m(Fe)+m(CuSO4)=m(FeSO4)+m(Cu)天平平衡参加反应的参加反应的各物质的质各物质的质量总和量总和生成的各物生成的各物质的质量总质的质量总和和质量守恒定律:质量守恒定律:水通电分解的微观展示水通电分解的微观展示化学变化的实质是:化学变化的实质是:分子原子分解为新分子重组反应前后原子的种类、...