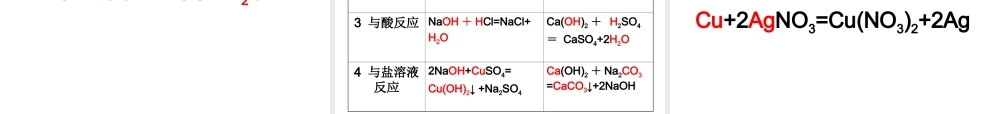
溶液的酸碱性酸性(碱性、中性)溶液的判断方法酸性物质(盐酸)碱性物质(石灰水)中性物质(食盐水)紫色石蕊试液无色酚酞试液蓝色石蕊试纸红色石蕊试纸红色红色红色无色蓝色蓝色不变色溶液酸碱性的强弱程度(溶液的酸碱性强弱)酸度?碱度?用PH试纸可以测定溶液的酸碱度。1、任何液体都有PH值;2、液体的PH值范围在0—14范围内;3、PH试纸只能测出液体的PH值的大致范围。4、液体的酸碱度与PH的关系:APH<7,溶液呈酸性,PH越小溶液的酸性越强;BPH=7,溶液呈中性;CPH>7,溶液呈碱性,PH越大溶液的碱性越强。浓硫酸和浓盐酸的物理性质浓硫酸浓盐酸溶质的化学式H2SO4HCl颜色、状态无色粘稠、油状液体无色液体气味无味有刺激性气味溶质质量分数96%—98%37%—38%密度比水大比水大敞开试剂瓶口发生的现象难挥发易挥发,在空气中易产生白雾其他有强烈的腐蚀性有腐蚀性酸的化学性质1.酸能与指示剂反应酸都能使紫色石蕊试剂变红色,使无色酚酞不变色。2.酸能与活泼的金属反应Zn+H2SO4=ZnSO4+H2↑Fe+2HCl=FeCl2+H2↑3.酸与金属氧化物反应Fe2O3+3H2SO4=Fe2(SO4)3+3H2OCuO+2HCl=CuCl2+H2O4.酸与碳酸盐等盐反应CaCO3+2HCl=CaCl2+CO2↑+H2OBaCl2+H2SO4=BaSO4↓+2HClAgNO3+HCl=AgCl↓+HNO35、酸能与碱反应(中和反应)HCl+NaOH=NaCl+H2O稀硫酸稀盐酸1与酸碱指示剂反应都能使紫色石蕊变红色,使无色的酚酞不变色2与金属反应Zn+H2SO4=ZnSO4+H2↑Fe+2HCl=FeCl2+H2↑3与金属氧化物反应Fe2O3+3H2SO4=Fe2(SO4)3+3H2OCuO+2HCl=CuCl2+H2O4与碱反应H2SO4+Ca(OH)2=CaSO4+2H2OHCl+NaOH=NaCl+H2O5与盐反应BaCl2+H2SO4=BaSO4↓+2HClCaCO3+2HCl=CaCl2+CO2↑+H2O氢氧化钠与氢氧化钙的物理性质化学式NaOHCa(OH)2俗名烧碱、火碱、苛性钠熟石灰、消石灰颜色状态白色块状固体白色粉未状固体溶解性极易溶于水放热可作干燥剂微溶于水腐蚀性有强腐蚀性有腐蚀性碱的化学性质1.碱溶液能与指示剂反应碱溶液都使紫色石蕊试剂不变色,使无色酚酞变红色。2.碱溶液与CO2、SO2等非金属氧化物反应CO2+Ca(OH)2=CaCO3↓+H2OSO2+2NaOH=Na2SO3+H2O3.碱溶液与硫酸铜等盐溶液反应Ca(OH)2+Na2CO3=CaCO3↓+2NaOH2NaOH+CuSO4=Cu(OH)2↓+Na2SO44.碱能与酸反应(中和反应)HCl+NaOH=NaCl+H2O氢氧化钠氢氧化钙1与指示剂反应都能使石蕊试液变蓝色,使无色酚酞变红色2与非金属氧化物反应2NaOH+SO2=Na2SO3+H2OCa(OH)2+CO2=CaCO3↓+H2O3与酸反应NaOH+HCl=NaCl+H2OCa(OH)2+H2SO4=CaSO4+2H2O4与盐溶液反应2N...