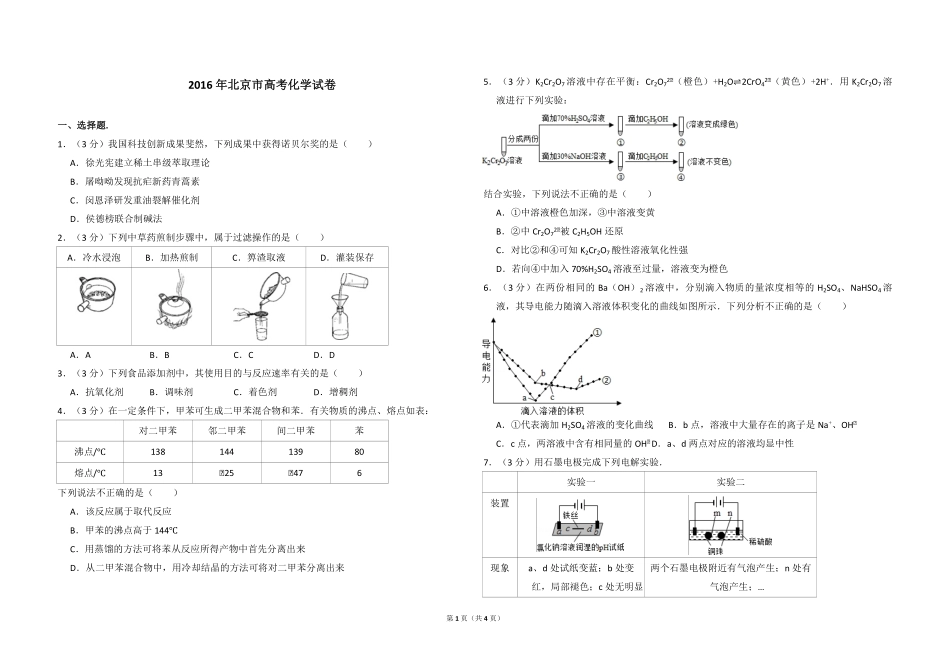
第1页(共4页)2016年北京市高考化学试卷一、选择题.1.(3分)我国科技创新成果斐然,下列成果中获得诺贝尔奖的是()A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素C.闵恩泽研发重油裂解催化剂D.侯德榜联合制碱法2.(3分)下列中草药煎制步骤中,属于过滤操作的是()A.冷水浸泡B.加热煎制C.箅渣取液D.灌装保存A.AB.BC.CD.D3.(3分)下列食品添加剂中,其使用目的与反应速率有关的是()A.抗氧化剂B.调味剂C.着色剂D.增稠剂4.(3分)在一定条件下,甲苯可生成二甲苯混合物和苯.有关物质的沸点、熔点如表:对二甲苯邻二甲苯间二甲苯苯沸点/℃13814413980熔点/℃13﹣25﹣476下列说法不正确的是()A.该反应属于取代反应B.甲苯的沸点高于144℃C.用蒸馏的方法可将苯从反应所得产物中首先分离出来D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来5.(3分)K2Cr2O7溶液中存在平衡:Cr2O72﹣(橙色)+H2O⇌2CrO42﹣(黄色)+2H+.用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是()A.①中溶液橙色加深,③中溶液变黄B.②中Cr2O72﹣被C2H5OH还原C.对比②和④可知K2Cr2O7酸性溶液氧化性强D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色6.(3分)在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是()A.①代表滴加H2SO4溶液的变化曲线B.b点,溶液中大量存在的离子是Na+、OH﹣C.c点,两溶液中含有相同量的OH﹣D.a、d两点对应的溶液均显中性7.(3分)用石墨电极完成下列电解实验.实验一实验二装置现象a、d处试纸变蓝;b处变红,局部褪色;c处无明显两个石墨电极附近有气泡产生;n处有气泡产生;…第2页(共4页)变化下列对实验现象的解释或推测不合理的是()A.a、d处:2H2O+2e﹣═H2↑+2OH﹣B.b处:2Cl﹣﹣2e﹣═Cl2↑C.c处发生了反应:Fe﹣2e﹣═Fe2+D.根据实验一的原理,实验二中m处能析出铜二、解答题(共4小题,满分58分)8.(17分)功能高分子P的合成路线如下:(1)A的分子式是C7H8,其结构简式是.(2)试剂a是.(3)反应③的化学方程式:.(4)E的分子式是C6H10O2.E中含有的官能团:.(5)反应④的反应类型是.(6)反应⑤的化学方程式:.(7)已知:2CH3CHO以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭...