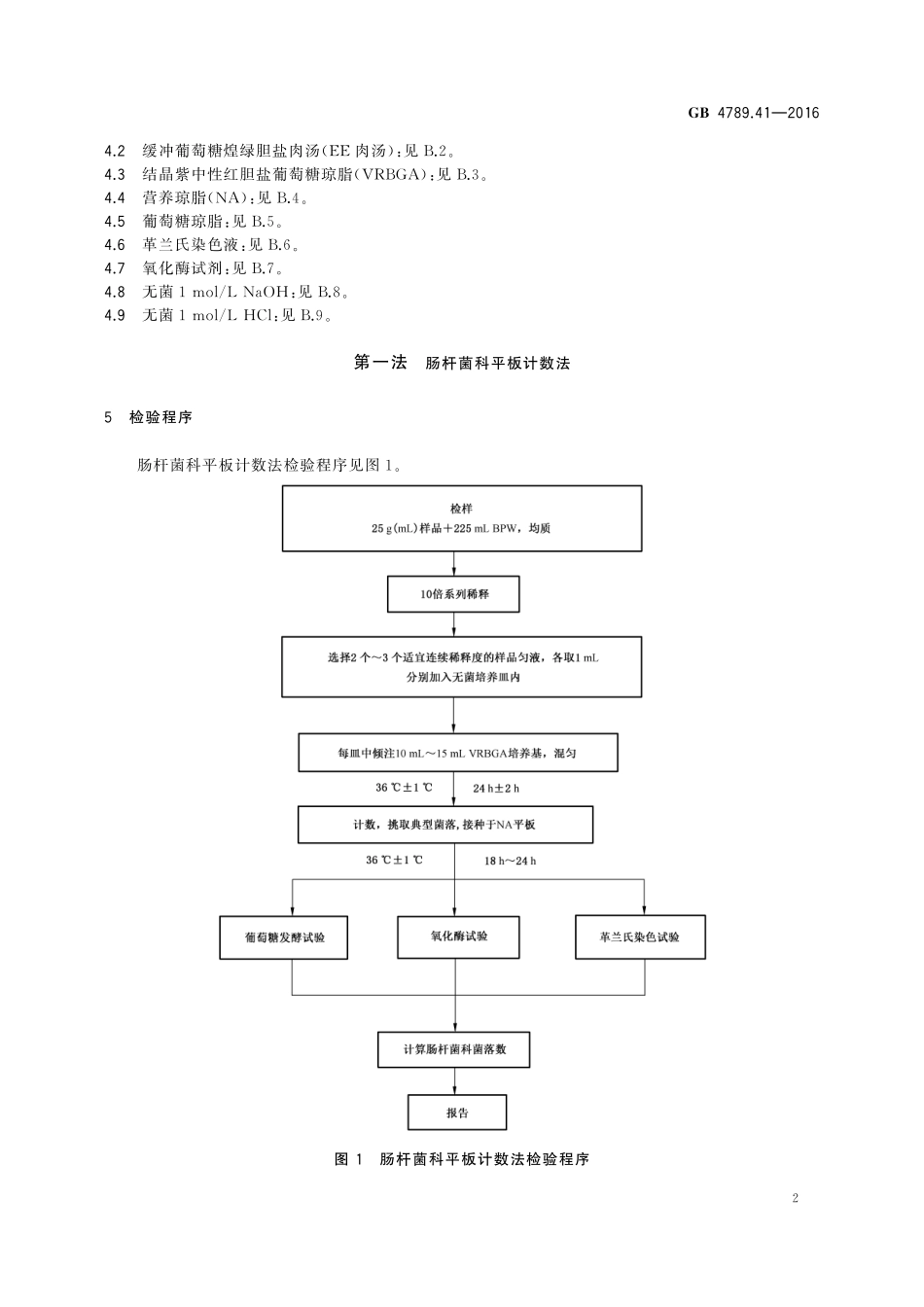
中华人民共和国国家标准GB4789.41—2016食品安全国家标准食品微生物学检验肠杆菌科检验2016-08-31发布2017-03-01实施中华人民共和国国家卫生和计划生育委员会发布GB4789.41—20161食品安全国家标准食品微生物学检验肠杆菌科检验1范围本标准规定了食品中肠杆菌科(Enterobacteriaceae)的检验方法。本标准第一法适用于肠杆菌科含量较高的食品中肠杆菌科的计数;第二法适用于肠杆菌科含量较低食品中肠杆菌科的计数。2术语和定义2.1肠杆菌科Enterobacteriaceae在给定条件下发酵葡萄糖产酸、氧化酶阴性的需氧或兼性厌氧革兰氏阴性无芽胞杆菌。2.2肠杆菌科计数EnumerationofEnterobacteriaceae按本标准规定方法,对每克或每毫升检样中的肠杆菌科进行计数。2.3最可能数mostprobablenumber;MPN基于泊松分布的一种间接计数方法。3设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:3.1恒温培养箱:36℃±1℃。3.2冰箱:2℃~5℃。3.3水浴箱:46℃±1℃。3.4天平:感量0.1g。3.5显微镜:10倍~100倍。3.6均质器。3.7振荡器。3.8无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头。3.9无菌锥形瓶或等效容器:容量150mL、500mL。3.10无菌培养皿:直径90mm。3.11无菌试管:18mm×180mm、15mm×150mm。3.12pH计或pH比色管或精密pH试纸。4培养基和试剂4.1缓冲蛋白胨水(BPW):见B.1。GB4789.41—201624.2缓冲葡萄糖煌绿胆盐肉汤(EE肉汤):见B.2。4.3结晶紫中性红胆盐葡萄糖琼脂(VRBGA):见B.3。4.4营养琼脂(NA):见B.4。4.5葡萄糖琼脂:见B.5。4.6革兰氏染色液:见B.6。4.7氧化酶试剂:见B.7。4.8无菌1mol/LNaOH:见B.8。4.9无菌1mol/LHCl:见B.9。第一法肠杆菌科平板计数法5检验程序肠杆菌科平板计数法检验程序见图1。图1肠杆菌科平板计数法检验程序GB4789.41—201636操作步骤6.1样品的稀释6.1.1固体和半固体样品:称取25g样品放入盛有225mLBPW的无菌均质杯中,8000r/min~10000r/min均质1min~2min,或放入盛有225mLBPW的无菌均质袋中,用拍击式均质器拍打1min~2min,制成1∶10的样品匀液。6.1.2液体样品:以无菌吸管吸取25mL样品放入盛有225mLBPW的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中,充分混匀,制成1∶10的样品匀液。6.1.3用1mL无菌吸管或微量移液器吸取1∶10样品匀液1mL,沿管壁缓缓注入盛有9mLBPW的无菌试管中(注意吸管或吸头尖端不应触及稀释液面),振摇试管或换用1支1mL无菌吸管反复吹打,使其混合均匀,制成1∶100的样品匀液。6.1.4按6.1.3操作程序,...